प्रोटीन का तात्विक विश्लेषण निम्नलिखित औसत मान देता है: 55% कार्बन, 7% हाइड्रोजन और 16% नाइट्रोजन; यह स्पष्ट है कि प्रोटीन एक दूसरे से भिन्न होते हैं, लेकिन उनकी औसत मौलिक संरचना ऊपर बताए गए मूल्यों से बहुत कम होती है। .
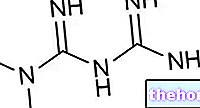
संवैधानिक रूप से, प्रोटीन प्राकृतिक α-एमिनो एसिड से बनने वाले मैक्रोमोलेक्यूल्स हैं; अमीनो एसिड एमाइड बॉन्ड के माध्यम से जुड़ते हैं जो एक एमिनो एसिड के एमिनो समूह और दूसरे ए-एमिनो एसिड के कार्बोक्सिल के बीच प्रतिक्रिया से स्थापित होता है।
इस बंधन (-CO-NH-) को पेप्टाइड बंधन भी कहा जाता है क्योंकि यह पेप्टाइड्स (संयोजन में अमीनो एसिड) को बांधता है:
प्राप्त एक डाइपेप्टाइड है क्योंकि यह दो अमीनो एसिड से बना होता है। चूंकि एक डाइपेप्टाइड में एक छोर पर एक मुक्त अमीनो समूह (NH2) और दूसरे पर एक कार्बोक्सिल (COOH) होता है, यह एक या एक से अधिक अमीनो एसिड के साथ प्रतिक्रिया कर सकता है और एक ही प्रतिक्रिया के साथ दाईं और बाईं ओर से श्रृंखला को लंबा कर सकता है। ऊपर देखा गया।
प्रतिक्रियाओं का क्रम (जो, वैसे, वास्तव में इतना सरल नहीं है) अनिश्चित काल तक जारी रह सकता है: जब तक एक बहुलक नहीं कहा जाता है पॉलीपेप्टाइड या प्रोटीन. पेप्टाइड्स और प्रोटीन के बीच का अंतर आणविक भार से जुड़ा होता है: आमतौर पर 10,000 से अधिक आणविक भार के लिए हम प्रोटीन की बात करते हैं।
छोटे प्रोटीनों को प्राप्त करने के लिए अमीनो एसिड को एक साथ बांधना एक मुश्किल काम है, हालांकि हाल ही में अमीनो एसिड से प्रोटीन बनाने की एक स्वचालित विधि विकसित की गई है जो उत्कृष्ट परिणाम देती है।
इसलिए, सबसे सरल प्रोटीन 2 अमीनो एसिड से बना होता है: अंतर्राष्ट्रीय सम्मेलन के अनुसार, प्रोटीन संरचना में अमीनो एसिड की क्रमांकित संख्या अमीनो एसिड से मुक्त ए-एमिनो समूह से शुरू होती है।
इस प्रोटीन के लिए कोडिंग) जो गैर-नगण्य रासायनिक कठिनाइयों का सामना करता है।
एडमैन डिग्रेडेशन के माध्यम से अमीनो एसिड के क्रमबद्ध अनुक्रम को निर्धारित करना संभव था: प्रोटीन फेनिलिसोथियोसाइनेट (एफआईटीसी) के साथ प्रतिक्रिया करता है; शुरू में α-एमिनो नाइट्रोजन डबल फेनिलिसोथियोसाइनेट पर हमला करता है जो थियोकार्बामाइल व्युत्पन्न बनाता है; बाद में, प्राप्त उत्पाद फेनिलथियोहाइडेंटोइन व्युत्पन्न देता है जो फ्लोरोसेंट है।
एडमैन ने सीक्वेंसर नामक एक मशीन तैयार की है जो स्वचालित रूप से गिरावट के लिए मापदंडों (समय, अभिकर्मकों, पीएच, आदि) को समायोजित करती है और प्रोटीन की प्राथमिक संरचना प्रदान करती है (इसके लिए उन्हें नोबेल पुरस्कार मिला)।
प्राथमिक संरचना प्रोटीन अणुओं के गुणों की पूरी तरह से व्याख्या करने के लिए पर्याप्त नहीं है; यह माना जाता है कि ये गुण आवश्यक रूप से स्थानिक विन्यास पर निर्भर करते हैं, जिसे प्रोटीन अणु विभिन्न तरीकों से मोड़ते हुए ग्रहण करते हैं: यानी, यह मानते हुए कि प्रोटीन की माध्यमिक संरचना के रूप में परिभाषित किया गया है।
प्रोटीन की द्वितीयक संरचना टिमटिमाती है, अर्थात यह गर्म करने से विघटित हो जाती है; तब प्रोटीन अपने कई विशिष्ट गुणों को खोते हुए स्वयं को नकारते हैं। 70 डिग्री सेल्सियस से ऊपर गर्म करने के अलावा, विकृतीकरण विकिरण या अभिकारकों की क्रिया (उदाहरण के लिए मजबूत एसिड से) के कारण भी हो सकता है।
ऊष्मीय प्रभाव के कारण प्रोटीन का विकृतीकरण देखा जाता है, उदाहरण के लिए, अंडे की सफेदी को गर्म करने से: यह अपने जिलेटिनस स्वरूप को खो देता है और एक अघुलनशील सफेद पदार्थ में बदल जाता है। हालांकि, प्रोटीन के विकृतीकरण से उनकी द्वितीयक संरचना नष्ट हो जाती है, लेकिन उनकी प्राथमिक संरचना अपरिवर्तित रहती है (विभिन्न अमीनो एसिड का संयोजन)।
प्रोटीन तृतीयक संरचना पर तब कार्य करते हैं जब उनकी श्रृंखला, हालांकि द्वितीयक संरचना के झुकने के बावजूद अभी भी लचीली होती है, इस तरह से मुड़ जाती है कि एक ठोस शरीर के आकार में एक विपरीत त्रि-आयामी व्यवस्था उत्पन्न होती है। तृतीयक संरचना के लिए जिम्मेदार सभी डाइसल्फ़ाइड बांडों से ऊपर हैं जो सिस्टीन-एसएच के बीच अणु के साथ बिखरे हुए स्थापित किए जा सकते हैं।
दूसरी ओर, चतुर्धातुक संरचना केवल दो या दो से अधिक उप-इकाइयों द्वारा निर्मित प्रोटीन से संबंधित है। हीमोग्लोबिन, उदाहरण के लिए, दो जोड़ी प्रोटीन से बना होता है (अर्थात, सभी चार प्रोटीन श्रृंखलाओं में) एक टेट्राहेड्रोन के कोने पर स्थित होता है ताकि एक गोलाकार संरचना को जन्म दिया जा सके; चार प्रोटीन श्रृंखलाएं आयनिक और बलों द्वारा एक साथ रखी जाती हैं। गैर-सहसंयोजक बंधन।
एक चतुर्धातुक संरचना का एक अन्य उदाहरण इंसुलिन का है, जो एक त्रिभुज के शीर्ष पर जोड़े में व्यवस्थित छह प्रोटीन उपइकाइयों से बना प्रतीत होता है, जिसके केंद्र में दो जस्ता परमाणु होते हैं।
रेशेदार प्रोटीन
वे एक निश्चित कठोरता वाले प्रोटीन होते हैं और दूसरे की तुलना में अधिक लंबी धुरी होते हैं; प्रकृति में अधिक मात्रा में मौजूद रेशेदार प्रोटीन कोलेजन (या कोलेजन) होता है।
एक रेशेदार प्रोटीन विभिन्न माध्यमिक संरचनाओं को ग्रहण कर सकता है: α-हेलिक्स, β-शीट और, कोलेजन के मामले में, ट्रिपल हेलिक्स; α-हेलिक्स सबसे स्थिर संरचना है, इसके बाद β-शीट है, जबकि तीनों में से सबसे कम स्थिर ट्रिपल हेलिक्स है।
अधिकार यदि, मुख्य कंकाल (नीचे से ऊपर की ओर उन्मुख) का अनुसरण करते हुए, दाहिने हाथ के पेंच के पेंच के समान एक आंदोलन किया जाता है; जबकि हेलिक्स का है बायां हाथ यदि आंदोलन बाएं हाथ के पेंच के पेंच के समान है। दाहिने हाथ में α-हेलीकॉप्टर -आर अमीनो एसिड के प्रतिस्थापन प्रोटीन की मुख्य धुरी के लंबवत होते हैं और बाहर की ओर होते हैं, जबकि बाएं में- हैंड ए-हेलिकॉप्टर -आर सब्स्टीट्यूट का सामना अंदर की ओर होता है। दाएं हाथ के ए-हेलिकॉप्टर बाएं हाथ वाले की तुलना में अधिक स्थिर होते हैं क्योंकि वटी-आर सी के बीच "कम बातचीत और कम स्टेरिक बाधा होती है। प्रोटीन में पाए जाने वाले सभी ए-हेलिकॉप्टर डेक्स्ट्रोरोटल होते हैं।
α-हेलिक्स की संरचना हाइड्रोजन बांड (हाइड्रोजन ब्रिज) द्वारा स्थिर होती है जो प्रत्येक अमीनो एसिड के कार्बोक्सिल समूह (-C = O) के बीच बनते हैं और अमीनो समूह (-NH) में बाद में चार अवशेष पाए जाते हैं। रैखिक अनुक्रम।
α-हेलिक्स संरचना वाले प्रोटीन का एक उदाहरण हेयर केराटिन है।
α-हेलिक्स संरचना को लंबा करके, α-हेलिक्स से β-शीट में संक्रमण किया जाता है; गर्मी या यांत्रिक तनाव भी α-हेलिक्स से β-शीट संरचना में जाने की अनुमति देता है।
आमतौर पर, एक प्रोटीन में, β-शीट संरचनाएं एक-दूसरे के करीब होती हैं क्योंकि प्रोटीन के कुछ हिस्सों के बीच इंटर-चेन हाइड्रोजन बॉन्ड स्थापित किए जा सकते हैं।
रेशेदार प्रोटीन में, अधिकांश प्रोटीन संरचना α-हेलिक्स या β-शीट में व्यवस्थित होती है।
गोलाकार प्रोटीन
उनके पास लगभग गोलाकार स्थानिक संरचना है (पॉलीपेप्टाइड श्रृंखला की दिशा में कई परिवर्तनों के कारण); अस्तित्व के कुछ हिस्सों को α-हेलिक्स या β-शीट संरचना में वापस खोजा जा सकता है और अन्य भाग, इसके बजाय, इन रूपों के कारण नहीं होते हैं: व्यवस्था यादृच्छिक नहीं बल्कि व्यवस्थित और दोहरावदार है।
अब तक जिन प्रोटीनों का उल्लेख किया गया है, वे पूरी तरह से सजातीय संविधान के पदार्थ हैं: यानी, संयुक्त अमीनो एसिड के शुद्ध क्रम; ऐसे प्रोटीन कहा जाता है सरल; प्रोटीन एक प्रोटीन भाग और एक गैर-प्रोटीन भाग (प्रोस्टेट समूह) से बना होता है जिसे प्रोटीन कहा जाता है संयुग्म.
, नाखूनों में, कॉर्निया में और आंख के लेंस में, कुछ अंगों (जैसे यकृत) के अंतरालीय स्थानों के बीच और इसी तरह।
इसकी संरचना इसे विशेष यांत्रिक क्षमता प्रदान करती है; इसमें उच्च लोच (जैसे टेंडन में) या उच्च कठोरता (जैसे।हड्डियों में) कार्य के आधार पर इसे निष्पादित करना होता है।
कोलेजन के सबसे जिज्ञासु गुणों में से एक इसकी संवैधानिक सादगी है: यह लगभग 30% प्रोलाइन और लगभग 30% ग्लाइसिन से बना होता है; अन्य 18 अमीनो एसिड को केवल शेष 40% प्रोटीन संरचना को साझा करना होता है। कोलेजन का अमीनो एसिड अनुक्रम उल्लेखनीय रूप से नियमित है: प्रत्येक तीन अवशेषों के लिए, तीसरा ग्लाइसिन है।
प्रोलाइन एक चक्रीय एमिनो एसिड है जिसमें आर समूह α-एमिनो नाइट्रोजन से बांधता है और यह इसे एक निश्चित कठोरता देता है।
अंतिम संरचना एक दोहराई जाने वाली श्रृंखला है जिसमें "हेलिक्स" का आकार होता है, कोलेजन श्रृंखला के भीतर, हाइड्रोजन बांड अनुपस्थित होते हैं। कोलेजन एक "बाएं हाथ का हेलिक्स है जिसमें एक पिच (हेलिक्स के एक मोड़ के अनुरूप लंबाई)" α-हेलिक्स से अधिक होती है; कोलेजन हेलिक्स इतना ढीला होता है कि तीन प्रोटीन श्रृंखलाएं एक दूसरे के चारों ओर लपेटने में सक्षम होती हैं, जिससे एक " एकल रस्सी: ट्रिपल हेलिक्स संरचना।
हालांकि, कोलेजन का ट्रिपल हेलिक्स α-हेलिक्स और β-शीट संरचना दोनों की तुलना में कम स्थिर होता है।
आइए अब उस तंत्र को देखें जिसके द्वारा कोलेजन का उत्पादन होता है; उदाहरण के लिए, रक्त वाहिका के टूटने पर विचार करें: यह टूटना जहाजों को बंद करने के उद्देश्य से असंख्य संकेतों के साथ होता है, इस प्रकार थक्का बनता है।
जमावट के लिए कम से कम तीस विशेष एंजाइमों की आवश्यकता होती है। थक्के के बाद ऊतक की मरम्मत के साथ जारी रखना आवश्यक है; घाव के करीब की कोशिकाएं भी कोलेजन का उत्पादन करती हैं। ऐसा करने के लिए, पहले एक जीन की अभिव्यक्ति को प्रेरित किया जाता है, अर्थात्, जीव जो एक जीन की जानकारी से शुरू होकर प्रोटीन का उत्पादन करने में सक्षम होते हैं (आनुवंशिक जानकारी mRNA पर स्थानांतरित होती है जो नाभिक को छोड़ देती है और राइबोसोम तक पहुंच जाती है। साइटोप्लाज्म जहां आनुवंशिक जानकारी का प्रोटीन में अनुवाद किया जाता है। फिर कोलेजन को राइबोसोम में संश्लेषित किया जाता है (यह लगभग 1200 अमीनो एसिड से बना एक बाएं हाथ का हेलिक्स जैसा दिखता है और इसका आणविक भार लगभग 150,000 d होता है) और फिर लुमेन में जमा हो जाता है जहां यह पोस्ट-ट्रांसलेशनल संशोधनों ("एमआरएनए द्वारा अनुवादित भाषा के संशोधन) करने में सक्षम एंजाइमों के लिए एक सब्सट्रेट बन जाता है; कोलेजन में, इन संशोधनों में कुछ साइड चेन, विशेष रूप से प्रोलाइन और लाइसिन के हाइड्रोक्साइलेशन शामिल होते हैं।
इन परिवर्तनों की ओर ले जाने वाले एंजाइमों की विफलता स्कर्वी का कारण बनती है: यह एक ऐसी बीमारी है जो शुरू में रक्त वाहिकाओं के टूटने, दांतों के टूटने का कारण बनती है जिसके बाद अंतःस्रावी रक्तस्राव और मृत्यु हो सकती है; यह लंबे समय तक भोजन के निरंतर उपयोग के कारण हो सकता है।
इसके बाद, अन्य एंजाइमों की कार्रवाई के कारण, अन्य संशोधन होते हैं जो प्रोलाइन और लाइसिन के हाइड्रॉक्सिल समूहों के ग्लाइकोसिडेशन में होते हैं (एक चीनी ओएच के ऑक्सीजन को बांधती है); ये एंजाइम लुमेन के अलावा अन्य क्षेत्रों में पाए जाते हैं, इसलिए प्रोटीन, संशोधनों के दौरान, एंडोप्लाज्मिक रेटिकुलम के अंदर स्थानांतरित होकर थैली (पुटिकाओं) में समाप्त हो जाता है जो खुद को बंद कर देते हैं और रेटिकुलम से अलग हो जाते हैं: उनके अंदर यह ग्लाइकोसिडेटेड प्रो निहित होता है। -कोलेजन मोनोमर; उत्तरार्द्ध गोल्गी तंत्र तक पहुंचता है जहां विशेष एंजाइम ग्लाइकोसिडेटेड प्रो-कोलेजन के कार्बोक्सी टर्मिनल भाग में मौजूद सिस्टीन को पहचानते हैं और विभिन्न श्रृंखलाओं को एक-दूसरे से संपर्क करने और डाइसल्फ़ाइड पुल बनाने का कारण बनते हैं: इस तरह से तीन श्रृंखलाएं ग्लाइकोसिडेटेड प्रो-कोलेजन एक साथ जुड़े हुए प्राप्त होते हैं और यह प्रारंभिक बिंदु है जिसमें तीन श्रृंखलाएं, इंटरपेनेट्रेटिंग, फिर, स्वचालित रूप से, ट्रिपल हेलिक्स को जन्म देती हैं। ग्लाइकोक्सीडेटेड प्रो-कोलेजन की तीन श्रृंखलाएं एक साथ जुड़ी हुई हैं, फिर एक पुटिका जो, खुद को घुटते हुए, गॉल्गी तंत्र से खुद को अलग कर लेता है, तीन श्रृंखलाओं को सेल की परिधि की ओर ले जाता है, जहां, उपद्रव के माध्यम से प्लाज्मा झिल्ली के साथ आयन, ट्राइमीटर को कोशिका से बाहर निकाल दिया जाता है।
अतिरिक्त सेलुलर स्पेस में, विशेष एंजाइम होते हैं, प्रो-कोलेजन पेप्टिडेस, जो सेल से निष्कासित प्रजातियों से हटाते हैं, 300 अमीनो एसिड के तीन टुकड़े (प्रत्येक हेलिक्स के लिए एक) l "एक, टर्मिनल कार्बोक्सी भाग से और तीन अमीनोटर्मिनल भाग से लगभग 100 अमीनो एसिड के टुकड़े (प्रत्येक हेलिक्स के लिए एक): एक ट्रिपल हेलिक्स रहता है जिसमें प्रति हेलिक्स लगभग 800 अमीनो एसिड होता है जिसे जाना जाता है ट्रोपोकोलेजन.
ट्रोपोकोलेजन में काफी कठोर छड़ का आभास होता है; विभिन्न ट्रिमर सहसंयोजक बंधों के साथ मिलकर बड़ी संरचनाएं देते हैं: सूक्ष्मतंतु. माइक्रोफाइब्रिल्स में, विभिन्न ट्रिमर को कंपित तरीके से व्यवस्थित किया जाता है; कई माइक्रोफाइब्रिल्स ट्रोपोकोलेजन बंडलों का निर्माण करते हैं।
हड्डियों में, कोलेजन तंतुओं के बीच, अंतरालीय स्थान होते हैं जिनमें कैल्शियम और मैग्नीशियम के सल्फेट और फॉस्फेट जमा होते हैं: ये लवण सभी तंतुओं को भी ढक लेते हैं; इससे हड्डियां सख्त हो जाती हैं।
टेंडन में, हड्डियों की तुलना में अंतरालीय रिक्त स्थान क्रिस्टल में कम समृद्ध होते हैं जबकि ट्रोपोकोलेजन की तुलना में छोटे प्रोटीन मौजूद होते हैं: यह टेंडन को लोच देता है।
ऑस्टियोपोरोसिस कैल्शियम और मैग्नीशियम की कमी के कारण होने वाली एक बीमारी है जो ट्रोपोकोलेजन फाइबर के अंतरालीय क्षेत्रों में लवण को ठीक करना असंभव बना देती है।